氧化铜自身具有氧化性,我们可以用氢气还原氧化铜。
灼热的氧化铜可以和氢气(H2)、碳(C)、一氧化碳(CO)等具有还原性物质反应,生成铜+X(氧化物)。
氢气还原氧化铜实验:
| 原理 | H2+CuO H2O+Cu H2O+Cu |
| 装置 | 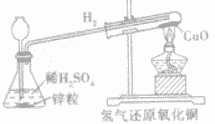 |
| 步骤 | ①先通氢气(直到盛氧化铜的试管内充满纯净的氢气) ②后点燃洒精灯加热 ③先熄灭洒精灯停止加热(当出现明显的实验现象后) ④后停止通氢气(等试管冷却后再停止) 简单记忆为“氢气早来晚走,酒精灯迟到早退” |
| 现象 | ①黑色氧化铜变成光亮红色 ②试管口处有小水珠 |
| 注意事项 | ①通氢气的导管必须伸入试管底部,保证与氧化铜充分反应 ②必须先通氢气后加热,否则可能会发生爆炸 ③停止加热后必须等试竹冷却后再停止通氢气,否则铜可能会重新被氧化 |
实验总结顺口溜:
氢气验纯试管倾
先通氢气后点灯
黑色变红水珠出
熄灭灯后再停氢
相关初中化学知识点:常用仪器的名称和选用
常用的实验仪器:
试管、烧杯、蒸发皿、坩埚、酒精灯、漏斗、洗气瓶、干燥管、
托盘天平、量筒、容量瓶、滴定管、玻璃棒、量气装置等。
常用仪器对比分析:
常见的化学仪器 | 主要用途 | ||
分类 | 名称 | 图示 | |
| 用于加热仪器 | 试管 |  | (1)用作少量试剂的反应容器,在常温或加热时使用 (2)作为小型气体发生器 (3)收集少量气体 |
| 蒸发皿 |  | 用于溶液的蒸发、浓缩 | |
| 燃烧匙 |  | 用于盛放可燃性固体物质进行燃烧实验 | |
| 烧杯 |  | (1)溶解物质配制溶液 (2)较大量试剂反应容器 (3)常温或加热使用 | |
| 锥形瓶,烧瓶(圆底,平底) |  | (1)用作较大量液体反应的容器和气体发生装置,在常温或加热时使用 (2)锥形瓶是蒸馏的接收容器 | |
| 酒精灯 |  | 用于加热 | |
| 盛放物质的仪器 | 集气瓶 |  | (1)收集和储存少量气体 (2)进行物质和气体之间的反应 |
| 滴瓶,滴管 |  | 滴瓶用于盛放少量液体试剂 | |
| 细口瓶 |  | 储存液体药品 | |
| 广口瓶 |  | 储存固体药品 | |
| 计量仪器 | 托盘天平 |  | 称量物质的质量(精确度为0.1g) |
| 量筒 |  | 量取一定体积的液体或间接测量气体的体积 | |
| 漏斗 | 普通漏斗 |  | 过滤,注入液体 |
| 长颈漏斗 |  | 用于注入液体 | |
| 分液漏斗 |  | (1)注入液体 (2)分液漏斗用于分离两种密度不同且互不相溶的液体 | |
| 夹持仪器 | 铁架台 |  | 固定和放置各种仪器 |
| 试管夹 |  | 夹持试管进行简单的加热试验 | |
| 坩埚钳 |  | 夹持坩埚或夹持热的蒸发皿等 | |
| 辅助仪器 | 水槽 |  | 排水集气 |
| 药匙 |  | 取用固体药品(粉末状或小颗粒状) | |
| 玻璃棒 |  | 搅拌液体,引流,沾取液体 | |
| 石棉网 |  | 用于烧杯或烧瓶加热时垫在底部,使仪器受热均匀 | |
| 试管刷 |  | 用于刷洗试管等玻璃仪器 | |
| 温度计 |  | 用于测量温度 | |
相关初中化学知识点:氧气的制取和收集
氧气的制取是初中化学的重点,也是历年中考的热点。我们不仅要学好氧气制取的知识,而且要触类旁通,逐步掌握实验室制取气体的一般思路和方法。中考对制取氧气的考查主要集中在药品选用、实验装置、操作步骤等方面。
实验室制取收集氧气:
| 过氧化氢制氧气 | 高锰酸钾制氧气 | |
| 药品和反应原理 | 2H2O2 2H2O+O2↑ 2H2O+O2↑ | 2KMnO4 K2MnO4 + MnO2 + O2↑ K2MnO4 + MnO2 + O2↑ |
| 发生装置 | 固液常温型 | 固体加热型 |
| 收集装置 | 氧气可用排水法收集,也可用向上排空气法收集 | |
| 整体装置图 |  | 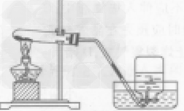 |
| 操作步骤 | ①检查装置气密性 ②再锥形瓶中装入二氧化锰 ③塞好带有长颈漏斗和导管的橡皮塞(长颈漏斗的下端一定在液面以下,否则氧气会从长颈漏斗中跑出来) ④向长颈漏斗中加入过氧化氢溶液 ⑤收集氧气 | ①检查装置气密性 ②将药品平铺在试管底部,用带导管的单孔橡皮塞塞紧试管口(用高锰酸钾制取氧气,还要在管口放一小团棉花) ③将试管固定在铁架台上 ④点燃酒精灯,预热后加热试管 ⑤当导管口有连续均匀的气泡冒出时开始收集气体 ⑥收集完毕,先将导管移出水面 ⑦熄灭酒精灯。加热高锰酸钾(或氯酸钾和二氧化锰的混合物)制氧气,用排水法收集,其操作步骤可概括为:“查”“装”“定”“点”“收”“离”“熄”7个字。可用谐音记忆为“茶庄定点收利息”。 |
| 注意事项 | ①伸入试管或锥形瓶中的导管应刚刚露出橡皮塞即可,否则不利于气体的导出。 ②用排水法收集氧气时,导管应刚伸人集气瓶口即可,过长不利于水的排出,气体不易收集满。 ③用向上排空气法收集氧气时,导管要伸入集气瓶的底部,否则不利于空气的排出,收集的气体不纯。 ④用长颈漏斗时,长颈漏斗末端应在液面以下,否则氧气会从长颈漏斗中逸出。 | ①药品要平铺在试管底部,均匀受热。 ②试管口要略向下倾斜,防止药品中湿存的水分受热后变成水蒸气,遇冷凝结成水倒流回试管底部,使试管炸裂。 ③铁架台的铁夹要夹在试管的中上部(或距离试管口1/3处)。 ④试管内的导管稍伸出橡皮塞即可,这样便于气体导出。 ⑤集气瓶充满水后倒放入水槽中(瓶口要在水面下)。 ⑥加热时要先使试管均匀受热,然后酒精灯外焰要对准药品所在部位加热。 ⑦用排水法收集气体时,应注意当气泡连续均匀冒出时再收集,否则收集的气体中混有空气,当集气瓶口有大盆气泡冒出时,证明已集满。 ⑧停止加热时,应先把导管从水里撤出,再撤掉酒精灯。如果先熄灭酒精灯,试管内气体温度降低,压强减小,水槽中的水就会被倒吸入热的试管内,使试管炸裂。 ⑨用高锰酸钾制氧气时,试管口要放一小团棉花,防止加热时高锰酸钾小颗粒进人导管。 ⑩盛氧气的集气瓶应盖上玻璃片正放,因为在相同状况下氧气的密度大于空气的密度,正放可减少气体的逸散。 |
相关初中化学知识点:常见仪器和装置的用途
“万能瓶”是最普通但很重要的一种仪器,它在化学实验中有广泛的应用。如果我们知道了,它的诸多功能,解答试题时就会得心麻手,事半功倍。
“万能瓶”在化学实验中有以下一些功能:
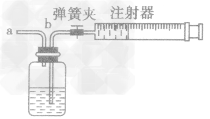
1.洗气(长进短出)
当制得的气体不纯时,或者要埘气体进行除杂时,都要想办法去掉杂质气体,这就是所谓的“洗气”,洗气瓶内装有吸收杂质的液体,混合气从长端进、短端出 (即长进短山或深入浅出)。如除去CO中混有的 CO2和水蒸气,应先通过 NaOH溶液,再通过浓硫酸。混合气体从A端进,两次洗气后CO从B端出(如图)。

2.集气(贮气)
①排空气法收集气体(如图所示):排空气法收集密度比空气大的气体(如O2或CO2等),气体从a端通入,空气从b端导出。排空气法收集密度比空气小的气体(如H2等),气体从b端通入,空气从a端导出

②排水法收集气体(如图所示) 瓶中盛满水,气体从b端进,水从a 端出。

3.量气(短入长出。如图所示)
瓶内先装满水,气体从a端进入,b 端接一个量筒,通过测量量筒内水的体积从而测得生成气体的体积。若气体能与氧气反应,可在瓶内水面上加一层油。

4.验气(检验或证明某气体,如图所示)
瓶内装有验证某气体所需试剂,检验时必须要有现象。气体流向是:长进短出,即a进b出。如检验CO中是否混有CO2,应通过Ca (OH)2溶液.观察有无白色沉淀生成。

5.安全瓶(长入短出,如图所示)
点燃可燃气体时,瓶内装少量水,将点燃的气体与发生装置产生的气体分隔开。

6.制取气体(如图所示)
打开橡皮塞装入固体,液体从b端流人(注意:瓶内的液面要液封b导管口)后立即夹紧橡皮管,产生的气体从a导管导出。如制取O2或CO2。
实验方案设计的几种方法:
1. 对比实验设计:
对比实验使实验设计中的一种基本思路,有利于实验现象的对比,有利于推理论证结论。如某学生欲探究碳酸具有酸性而二氧化碳不具有酸性,按下图进行实验。
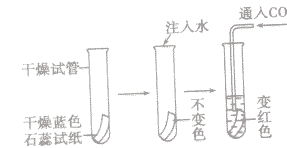
2. 控制变量实验设计:
一个问题常常受多方面的因素制约,为了研究每一个因素对问题的影响程度.常常采取控制变量法逐个检验,每一个现象只说明一个问题,换一个条件再检验其他因素的影响。综合各个因素对问题的影响作出综合性的判断,如课本上燃烧条件实验设计和铁的生锈条条件设计是控制变量实验设计。
解答实验设计题的方法技巧:
(1)解答实验探究题首先应具备良好的实验操作基本知识,懂得操作的一般步骤和原理,熟悉相关物质的性质、制备原理和变化规律。同时要读懂题,明确实验目的,充分利用题中所给信息(如装置、药品、题干中描述的目的等),分析题意设计相关的猜想(假设),提出问题,设汁实验的程序,再分现象得出相关的结论和启示、解答实验题还应具备整体、全局意识,即审题时要先统观全局,逐字逐句把整道题审读一遍再细致地读懂每一步要求,这样才能在答题时少丢分或不丢分。
(2)实验方案设计题的解答思路与方法
①明确实验目的――明确实验的目的和要求,弄清题给的新信息。
②选择仪器、药品――选择合理的化学仪器和药品。
③设计装置、步骤一一设计出合理的实验装置和实验操作步骤
④记录现象、数据一一一全面、及时而准确地记录实验过程中的数据和现象。
⑤分析得出结论一根据实验的观象和记录的数据,通过分析、计算、列图表、推理等处理,得出正确的结论。
化学实验的典型装置:
(1)防倒吸装置:在水中溶解性很大的气体(如HCl,NH3等),特别要注意防倒吸(如下图所示)
(2)防污染装置:燃烧法,吸收法,和袋装法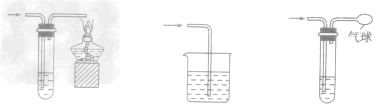
(3)气体的测量装置
(4)干燥除杂装置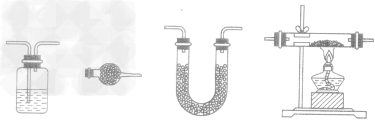
(5)启普发生器原理反应装置
(6)常见的电解水装置
自制电解水装置:
(1)用一个大瓶子,截去瓶底,留瓶口一段约高8~10cm。瓶口配一胶塞,由里向外塞紧。用镀铬曲别针伸直一段由塞子上扎出,在瓶塞露头处连接导线,做成电解槽如下图I。
(2)也可用普通玻璃杯(或烧杯)作电解槽。把硬导线跟镀铬曲别针用焊锡焊牢,导线用塑料管套起来,管口可以用蜡或沥青封住。把做好的电极同定在一块木板上,如图Ⅱ,电极的硬导线可以架在玻璃杯(电解槽)的壁上,集气管倒放在木板上。其他电解水装置如下图。
相关初中化学知识点:盐的性质
盐的定义:
盐是指由金属离子(或钱根离子)和酸根离子构成的化合物,盐在溶液里能解离成金属离子(或钱根离子)和酸根离子。根据阳离子不同,可将盐分为钠盐、钾盐、钙盐、钱盐等,根据阴离子不同,可将盆分为硫酸盐、碳酸盐,硝酸盐等。
生活中常见的盐有:
氯化钠(NaCl),碳酸钠 (Na2CO3)、碳酸氧钠(NaHCO3)、碳酸钙和农业生产上应用的硫酸铜(CuSO4)。
盐的物理性质:
(1)盐的水溶液的颜色常见的盐大多数为白色固体,其水溶液一般为无色。但是有些盐有颜色,其水溶液也有颜色。例如:胆矾(CuSO4・5H2O)为蓝色,高锰酸钾为紫黑色;含Cu2+的溶液一般为蓝色,含Fe2+的溶液一般为浅绿色,含Fe3+的溶液一般为黄色。
(2)盐的溶解性记忆如下钾钠硝钱溶水快(含K+,Na+,NH4+,NO3-的盐易溶于水);硫酸盐除钡银钙(含SO42-的盐中,Ag2SO4, CaSO4微溶,BaSO3难溶)都易溶;氯化物中银不溶(含 Cl-的盐中,AgCl不溶于水,其余一般易溶于水);碳酸盐溶钾钠钱[含CO32-的盐,Na2CO3、(NH4)2CO3、 K2CO3易溶,Na2CO3微溶,其余难溶〕。
盐的化学性质:
(1)盐+金属一另一种盐+另一种金属(置换反应),例如:Fe+CuSO4==FeSO4+Cu
规律:反应物中盐要可溶,金属活动性顺序表中前面的金属可将后面的金属从其盐溶液中置换出来(K, Ca,Na除外)。
应用:判断或验证金属活动性顺序和反应发生的先后顺序。
(2)盐+酸→另一种盐+另一种酸(复分解反应),例如;HCl+AgNO3==AgCl↓+HNO3。
规律:反应物中的酸在初中阶段一般指盐酸、硫酸、硝酸。盐是碳酸盐时可不溶,若是其他盐,则要求可溶。应用:实验室制取CO2,CO32-、Cl-,SO42-的检验。
(3)盐+碱→另一种盐+另一种碱(复分解反应)
规律:反应物都可溶,若反应物中盐不为按盐,生成物其中之一为沉淀或水。
应用:制取某种碱,例如:Ca(OH)2+Na2CO3== CaCO3↓+2NaOH。
(4)盐+盐→另外两种盐
规律:反应物都可溶,生成物至少有一种不溶于水。
应用:检验某种离子或物质。例如:NaCl+AgNO3 =AgCl↓+NaNO3(可用于鉴定Cl-);Na2SO4+BaCl2==BaSO4↓+2NaCl(可用与鉴定SO42-)
几种常见盐的性质及用途比较如下表:
| 氯化钠 | 碳酸钠 | 碳酸氢钠 | 碳酸钙 | 硫酸铜 | |
| 化学式 | NaCl | Na2CO3 | NaHCO3 | CaCO3 | CuSO4 |
| 俗称 | 食盐 | 纯碱、苏打 | 小苏打 | ―― | ―― |
| 物理性质 | 白色固体,易溶于水。水溶液有咸味,溶解度受温度影响小 | 白色固体,易溶于水 | 白色固体,易溶于水 | 白色固体,不溶于水 | 白色固体,易溶于水,溶液为蓝色,有毒 |
| 化学性质 | 水溶液显中性 AgNO3+NaCl==AgCl↓+NaNO3 | 水溶液显碱性 Na2CO3+2HCl==2NaCl+H2O+CO2↑ Na2CO3+Ca(OH)2==CaCO3↓+2NaOH | 水溶液显碱性 NaHCO3+HCl==NaCl+H2O+CO2↑ | CaCO3+2HCl==CaCl2+H2O+CO2↑ | CuSO4+5H2O==CuSO4・5H2O CuSO4+Fe==FeSO4+Cu CuSO4+2NaOH==Cu(OH)2↓+Na2SO4 |
| 用途 | 作调味品和防腐剂,医疗上配置生理盐水。重要的化工原料 | 制烧碱,广泛用于玻璃、纺织、造纸等工业 | 焙制糕点的发酵粉的主要成分,医疗上治疗胃酸过多 | 实验室制取CO2,重要的建筑材料,制补钙剂 | 农业上配制波尔多液,实验室中用作水的检验试剂,精炼铜 |
易错点:
①“食盐是盐是对的,但“盐就是食盐”是错误的,化学中的“盐”指的是一类物质。
②石灰石和大理石的主要成分是碳酸钙,它们是混合物,而碳酸钙是纯净物。
③日常生活中还有一种盐叫亚硝酸钠,工业用盐中常含有亚硝酸钠,是一种自色粉末,有咸味,对人体有害,常用作防腐保鲜剂。
④CuSO4是一种白色固体,溶于水后形成蓝色的CuSO4溶液,从CuSO4溶液中结品析出的晶体不是硫酸铜,而是硫酸铜晶休,化学式为CuSO4・5H2O,俗称胆矾或蓝矾,是一种蓝色固体。硫酸铜与水结合也能形成胆矾,颜色由白色变为蓝色.利用这种特性常用硫酸铜固体在化学实验中作检验水的试剂。
盐的命名:
(1)只有两种元素组成的盐,读作“某化某”,如 NaCl读作氯化钠,AgI读作碘化银。
(2)构成中含有酸根的,读作“某酸某”。如Na2CO3、ZnSO4、AgNO3、KMnO4、KClO3分别读作:碳酸钠、硫酸锌、硝酸银、高锰酸钾、氯酸钾。
(3)含铵根的化合物,读作“某化铵”或“某酸铵”。如NH4Cl、(NH4)2SO4读作:氯化铵、硫酸铵。
(4)其他:Cu2(OH)2CO3读作“碱式碳酸铜”, NaHSO4读作“硫酸氢钠”, NaHCO3读作“碳酸氢钠”。
风化:
风化是指结晶水合物在室温和干燥的条件下失去结晶水的现象,这种变化属于化学反应。如 Na2CO3・10H2O==Na2CO3+10H2O;CaSO4・2H2O ==CaSO4+2H2O。
侯氏制碱法:
我国化工专家侯德榜于1938-1940年用了三年时间,成功研制出联合制碱法,后来命名为“侯氏联合制碱法”。其主要原理是:
NH3+CO2+H2O== NH4HCO3
NH4HCO3+NaCl ==NaHCO3↓+NH4CI
2NaHCO3==Na2CO3+H2O+CO2↑
(1)NH3与H2O,CO2反应生成NH4HCO3。
(2)NH4HCO3与NaCl反应生成NaHCO3沉淀。主要原因是NaHCO3的溶解度较小。
(3)在第(2)点中过滤后的滤液中加入NaCl,由于 NH4CI在低温时溶解度非常低,使NH4Cl结晶析出,可做氮肥。
(4)加热NaHCO3得到Na2CO3.
优点:保留了氨碱法的优点,消除了它的缺点,提高了食盐的利用率,NH4Cl可做氮肥,同时无氨碱法副产物CaCl2毁占耕田的问题。
本文来自:逍遥右脑记忆 http://www.jiyifa.net/chuzhong/269782.html
相关阅读:初中化学总结:化学易错字及易混淆名词



